Що таке валентність
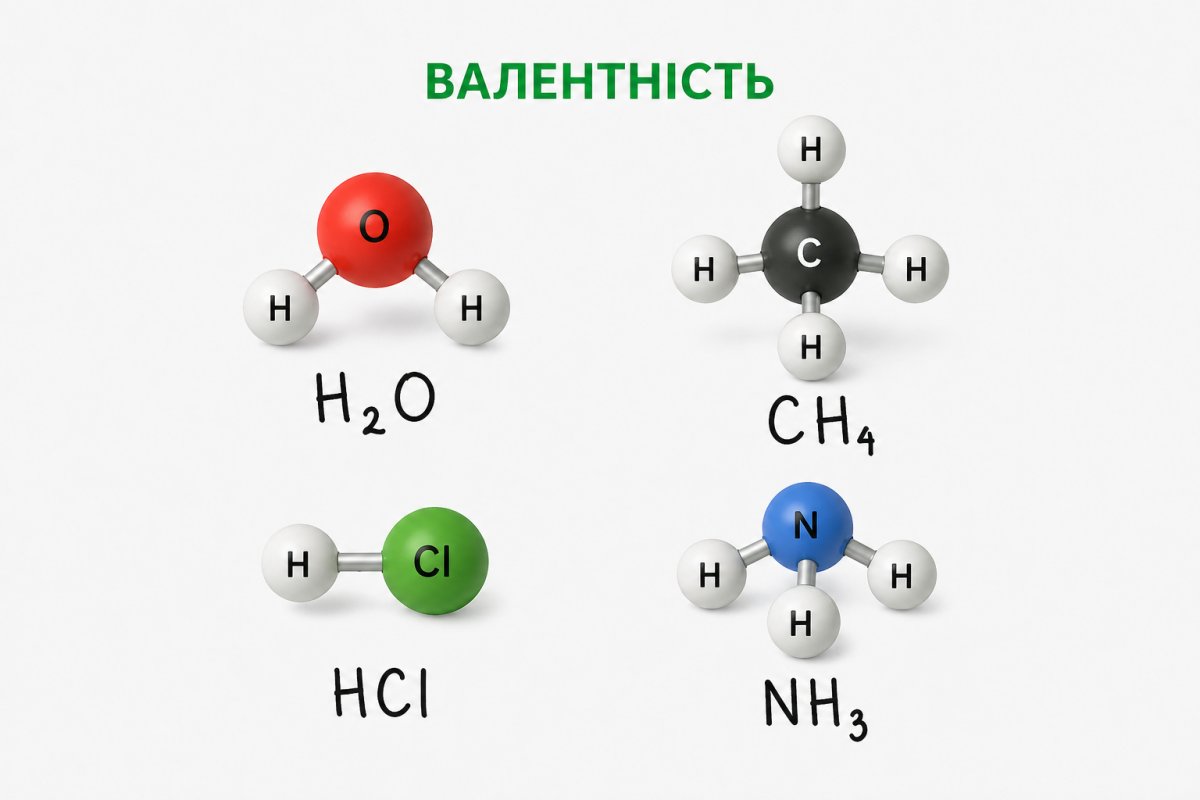
Валентність це здатність атома утворювати певну кількість хімічних зв’язків з іншими атомами. Вона залежить від будови електронної оболонки і прагнення атома до стабільності.
Уявіть атом як людину з відкритими руками. Кількість рук і є його валентність. Чим більше "рук", тим більше зв’язків він може утворити. Але важливо не лише число, а й те, з ким саме утворюється зв’язок. Один і той самий елемент у різному оточенні поводиться інакше, ніби змінює характер.
Валентність це не просто цифра, а ключ до розуміння того, як утворюються речовини навколо нас
Якщо дивитися глибше, валентність варто відчувати через приклади. Коли ви бачите формулу, намагайтеся уявити структуру молекули. Це допомагає не просто рахувати, а розуміти. Корисно час від часу виписувати прості формули і перевіряти їх логіку, навіть без підручника.
Основні принципи валентності
- валентність визначає кількість зв’язків атома
- вона залежить від кількості електронів на зовнішньому рівні
- може змінюватися у різних сполуках
- часто пов’язана зі ступенем окиснення
Коли працюєте з цими принципами, варто не заучувати їх механічно, а співвідносити з реальними прикладами. Наприклад, порівняйте воду і вуглекислий газ. Ви швидко побачите різницю в поведінці елементів.
Постійна і змінна валентність

- Постійна валентність характерна для елементів як Натрій або Кальцій
- Змінна валентність властива Перехідним металам і деяким неметалам
- Один елемент може мати різні значення у різних сполуках
- Це ускладнює, але робить хімію цікавішою
Щоб легше орієнтуватися, зручно групувати елементи. Наприклад, метали лужної групи майже завжди мають валентність I. А ось елементи як Сульфур або Нітроген варто розглядати у кількох варіантах. Такий підхід значно економить час при розв’язанні задач.
Як визначити валентність за формулою
Коли перед вами хімічна формула, вона вже містить підказку. Важливо лише правильно її прочитати. Кожен індекс показує кількість атомів, а разом вони формують баланс зв’язків.
Наприклад, у воді H₂O Оксиген має валентність II, а Гідроген I. Але якщо взяти іншу речовину, правила залишаються ті самі, змінюються лише числа.
Метод через відому валентність
- знайдіть елемент з відомою валентністю
- помножте валентність на кількість атомів
- поділіть результат на кількість атомів іншого елемента
Розглянемо приклад CO₂
- Оксиген має валентність II
- У формулі 2 атоми Оксигену
- 2 × II = IV
- Карбон має валентність IV
Якщо один елемент відомий, другий завжди можна знайти через просту логіку
Коли тренуєтесь, намагайтеся вирішувати приклади без підглядання у таблиці. Це розвиває швидкість мислення. Якщо виникає сумнів, спробуйте скласти кілька альтернативних варіантів і перевірити, який з них логічно підходить.
Розширена таблиця валентностей
| Елемент | Валентність |
|---|---|
| H | I |
| O | II |
| Na | I |
| K | I |
| Li | I |
| Ca | II |
| Mg | II |
| Ba | II |
| Al | III |
| B | III |
| C | II, IV |
| Si | IV |
| N | I, II, III, IV, V |
| P | III, V |
| S | II, IV, VI |
| Cl | I, III, V, VII |
| Fe | II, III |
| Cu | I, II |
| Zn | II |
| Ag | I |
| Au | I, III |
| Cr | II, III, VI |
| Mn | II, IV, VII |
Щоб ефективно працювати з таблицею, корисно не просто читати її, а періодично відтворювати по пам’яті. Почніть з найчастіших елементів і поступово додавайте нові. Це значно пришвидшує роботу з формулами.
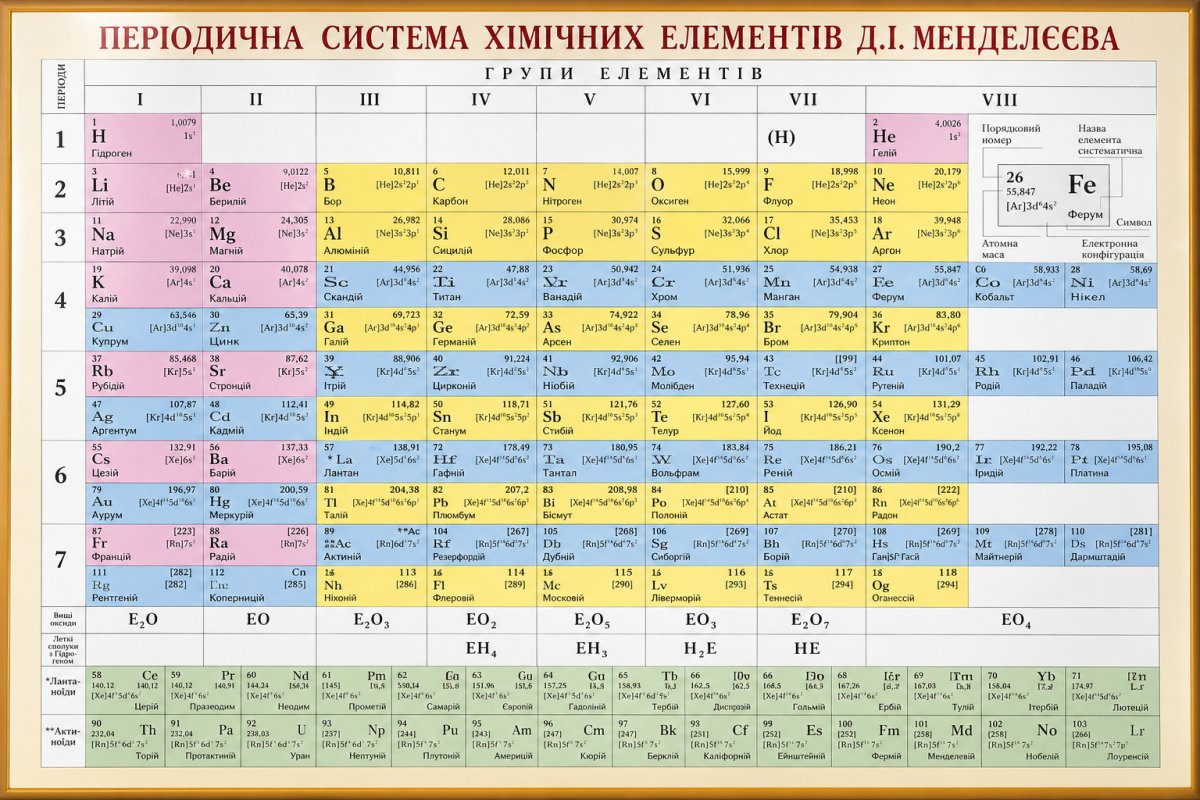
Як визначити валентність за періодичною системою
Періодична система хімічних елементів дає підказки щодо валентності.
Елементи головних підгруп мають передбачувану поведінку. Їх валентність часто дорівнює номеру групи або обчислюється через нього. Це як карта, яка допомагає орієнтуватися навіть без формули.
Правила для головних підгруп
- для металів валентність дорівнює номеру групи
- для неметалів валентність визначається як 8 мінус номер групи
- винятки можливі у складних сполуках
Коли працюєте з періодичною системою, дивіться не лише на групу, а й на період. Це дає додаткове розуміння будови атома. З часом ви почнете помічати закономірності без підрахунків.
Приклади визначення
- Натрій у 1 групі має валентність I
- Магній у 2 групі має валентність II
- Хлор у 7 групі може мати I, III, V, VII
- Сульфур може проявляти II, IV, VI
Якщо складно запам’ятати варіанти, створіть власні асоціації або приклади. Це значно підвищує ефективність навчання і допомагає уникнути плутанини.
Валентність у складних сполуках
Коли формули стають довшими, логіка стає ще важливішою. Тут валентність допомагає зберегти баланс і гармонію між атомами.
Алгоритм визначення
- визначте відомі елементи
- знайдіть їх загальну валентність
- урівняйте суму зв’язків між атомами
- зробіть висновок для невідомого елемента
Розглянемо Al₂O₃
- Оксиген має валентність II
- 3 × II = VI
- 2 атоми Алюмінію
- VI ÷ 2 = III
У складних формулах валентність працює як ваги, де кожна сторона повинна бути врівноважена
Коли працюєте зі складними формулами, не поспішайте. Краще розкласти задачу на кроки і перевіряти кожен етап. Якщо результат виглядає дивно, поверніться і знайдіть помилку. Такий підхід формує точність.
Типові помилки
- плутанина між валентністю і ступенем окиснення
- ігнорування індексів у формулі
- неправильне визначення відомих значень
- відсутність перевірки результату
Щоб уникнути цих помилок, корисно після кожного прикладу робити коротку перевірку. Запитайте себе, чи сходиться баланс зв’язків. Це займає кілька секунд, але економить багато часу.
Практичні поради для швидкого визначення

Іноді потрібно визначити валентність швидко, наприклад на уроці або іспиті. Тут допомагають прості прийоми, які з часом стають автоматичними.
Швидкі орієнтири
- запам’ятайте валентність H, O, Na, Ca
- використовуйте таблицю як основу
- звертайте увагу на індекси
- перевіряйте логіку розрахунків
Поступово ви почнете помічати, що багато задач повторюються. Використовуйте це як перевагу. Чим більше знайомих ситуацій, тим швидше приймається рішення.
Тренування через приклади
- NH₃
- H₂SO₄
- Fe₂O₃
- CaCl₂
Практика перетворює складні формули на зрозумілу і навіть передбачувану систему
Спробуйте не просто розв’язувати приклади, а пояснювати їх уголос. Це допомагає закріпити знання і краще зрозуміти логіку. З часом валентність перестає бути темою для запам’ятовування і стає інструментом, яким ви користуєтесь впевнено і легко.















